Железо
Содержание:
- Препараты трехвалентного железа
- Биохимический анализ крови
- Физические свойства
- Сферы применения
- Разновидности сплавов на основе железа
- Сферы применения
- Вещества со степенью окисления железа (III)
- История – краткая справка
- Железо как обозначается в анализе крови
- Продукты, содержащие феррум
- По каким признакам можно заподозрить нехватку железа в организме
- Тотема
- Признаки нехватки железа в организме
- Ферретаб комп.
- Области применения
- Значение железной руды и сферы, в которых она используется
- Классификация металлов по температуре плавления
- Химический состав
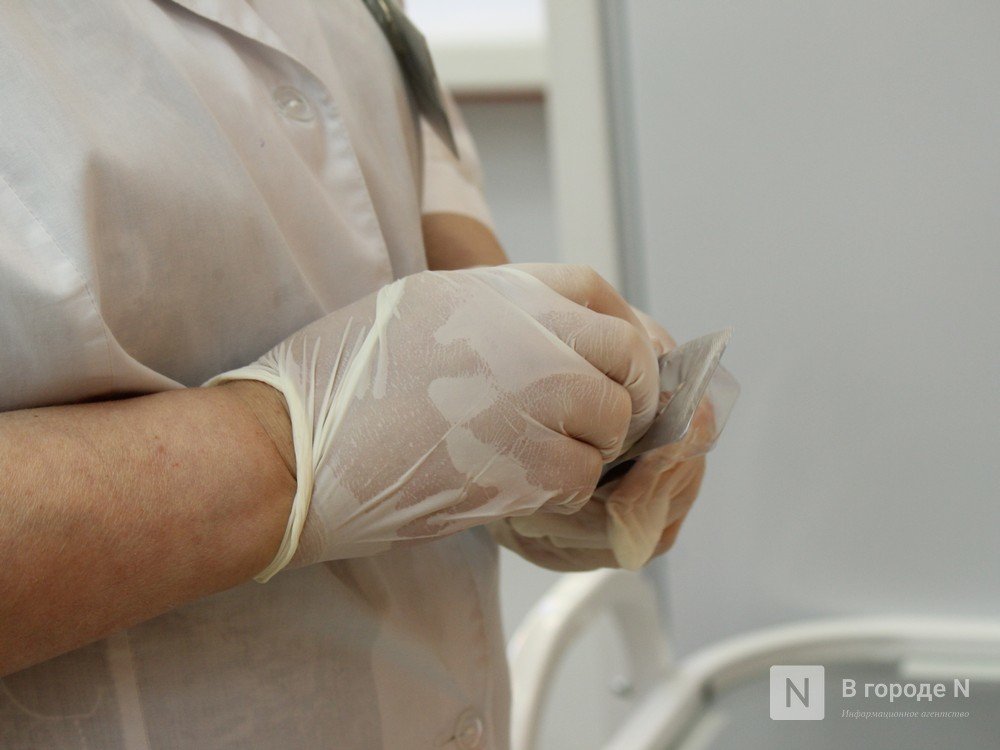
Препараты трехвалентного железа
Преимущества препаратов трехвалентного железа
- Малотоксичны. Их невозможно передозировать.
- Лучше переносятся.
- Их можно принимать и до, и во время, и после еды, не боясь получить воспаление или изъязвление слизистой ЖКТ.
- Меньше лекарственных взаимодействий.
- Меньше взаимодействий с пищевыми продуктами.
Недостатки препаратов трехвалентного железа
Действуют медленнее, поэтому сроки лечения увеличиваются.
Как я уже говорила вам в прошлый раз, если требуется быстро поднять железо (предстоит операция, тяжелая степень анемии и пр.), в начале лечения врач назначит, скорее всего, препарат двухвалентного железа. В дальнейшем он может перевести больного на препарат трехвалентного железа, если он плохо переносит двухвалентное.
Разберем особенности некоторых популярных препаратов этой группы.
Биохимический анализ крови
Биохимический анализ является подвидом общего анализа крови и проводится в случаях, когда в общем анализе крови были обнаружены отклонения показателей от нормальных значений. Анализ позволяет уточнить поставленный диагноз или скорректировать назначенное лечение. В биохимическом анализе крови обозначения представляют собой буквенную аббревиатуру либо общее название показателя. Рассмотрим расшифровку обозначений биохимического анализа крови:
- Общий белок. Представляет собой суммарное количество белков в крови, участвует в свертываемости крови, транспортировании различных веществ к органам и тканям. В норме соответствует значениям 64-84 г/л. Превышение нормы может говорить об инфекциях, артрите, онкологических заболеваниях.
- Glu — глюкоза. В норме не превышает 3,30-5,50 ммоль/л. Повышение показателя сигнализирует о развитии сахарного диабета. В организме глюкоза отвечает за углеводный обмен.
- Мочевина. Образуется при распаде белков. В норме составляет 2,5-8,3 ммоль/л. Значение показателя увеличивается при заболеваниях почек, непроходимости кишечника, болезнях мочевыводящих системы.
- ЛПНП, ЛПВП обозначают в биохимическом анализе крови уровень холестерина, который принимает участие в обмене жиров, выработке витамина D, оказывает влияние на функционирование половых гормонов. Границы нормы составляют 3,5-6,5 ммоль/л. Данный показатель повышается при атеросклерозе, сердечно-сосудистых болезнях, заболеваниях печени.
- BIL – билирубин. Пигмент красно-желтого цвета, образуется после распада гемоглобина. Общий билирубин состоит из непрямого и прямого билирубина, в норме соответствует значениям 5-20 мкмоль/л. Сильное увеличение показателя свидетельствует о недостатке витамина В12, развитии желтухи, раковых заболеваний.
- Креатинин. Является индикатором работы почек, принимает участие в энергетическом обмене тканей. Уровень нормы зависит от массы тела человека и составляет 53-115 мкмоль/л. Как правило, увеличение этого показателя свидетельствует о почечной недостаточности.
- α-амилаза, amylase — амилаза. Способствует расщеплению и перевариванию углеводов. Нормальное значение для α-амилазы – 28-100 ед/л, для панкреатической амилазы – 0-50 ед./л. Увеличение показателя может свидетельствовать о перитоните, панкреатите, сахарном диабете и некоторых других заболеваниях.
- lipase — липаза. Фермент поджелудочной железы, расщепляющий жиры. В норме не превышает 190 ед/л. При расшифровке обозначений биохимического анализа крови увеличение показателя будет свидетельствовать о развитии заболеваний поджелудочной железы.
- АлАТ (АЛТ) – аланинаминотрансфераза. Особый фермент, используемый для диагностики работы печени. АЛТ появляется в крови, если разрушаются клетки печени, сердца, почек. В норме показатель не должен превышать 41 ед./л. у мужчин и 31 ед./л. у женщин.
Мы привели расшифровку обозначений биохимического анализа крови в отношении наиболее общих и стандартных показателей. Вместе с этими обозначениями в анализе крови на биохимию встречаются и другие показатели: гамма-ГТ, фосфатаза щелочная, ЛПНП (липопротеины низкой плотности), триглицериды, К+ (калий), Na (натрий), Cl (хлор), С-реактивный белок, железо. Данные значения, отклоняющиеся от нормы, также могут свидетельствовать о нарушениях в организме человека.
Как видите, зная обозначения в анализах крови и границы нормальных значений, можно самостоятельно определить, находится ли показатель в пределах нормы. Однако не забывайте, что сделать правильную расшифровку анализа может сделать только врач.
Физические свойства
Как простое вещество, железо физические свойства имеет с ярко выраженным металлизмом. То есть это серебристо-белый с серым оттенком металл, обладающий высокой степенью ковкости и пластичности и высокой температурой плавления и кипения. Если рассматривать характеристики более подробно, то:
- температура плавления — 1539 С;
- кипения — 2862 С;
- активность — средняя;
- тугоплавкость — высокая;
- проявляет ярко выраженные магнитные свойства.
В зависимости от условий и различных температур, существует несколько модификаций, которые образует железо. Физические свойства их различаются от того, что разнятся кристаллические решетки.
- Альфа-форма, или феррит, существует до температуры в 769 С.
- От 769 до 917 С — бета-форма.
- 917-1394 С — гамма-форма, или аустенит.
-
Свыше 1394 С — сигма-железо.
Все модификации имеют различные типы строения кристаллических решеток, а также отличаются магнитными свойствами.
Сферы применения
Этот материл применяется в разных отраслях промышленности:
- Смеси и однородный металл применяются в машиностроении. Из них изготавливаются внутренние детали, корпуса, подвижные механизмы.
- Судостроение, самолётостроение, ракетостроение.
- Строительство — изготовление крепежей, расходных материалов.
- Приборостроение — изготовление электроники для дома.
- Радиоэлектроника — создание элементов для электроприборов.
- Медицина, станкостроение, химическая промышленность.
- Изготовление оружия.
Если для чего-то не подходит однородный материал, подойдут соединения на его основе, характеристики которых значительно отличаются.
Разновидности сплавов на основе железа
Сплав железа — это соединение, которое состоит из основного металла и дополнительных примесей. Соединения на основе этого материала называются чёрными металлами. К ним относятся:
- Сталь — соединение углерода с другими элементами. Углерода в составе сплава может содержаться до 2.14%. Выделяют конструкционные углеродистые, строительные, специальные и легированные стали.
- Чугун — смесь, которая пользуется огромной популярностью. Соединения могут содержать до 3,5% углерода. Дополнительно смеси содержать марганец, фосфор, серу.
- Перлит — смесь на основе железа. Содержит не более 0.8% углерода.
- Феррит — его называют чистым материалом. Связанно это с низким содержанием углерода, сторонних примесей (около 0.04%).
- Цементит — химическое соединение железа с углеродом.
- Аустенит — соединение с содержанием углерода до 2.14%. Дополнительно имеет сторонние примеси.
 Легированная сталь
Легированная сталь
Состав и структура сплавов
Из-за большого количество соединений на основе железа была разработана маркировка, по которой можно отделить стали с высоким содержанием углерода от менее углеродистых, определить наличие основных легирующих элементов в составе материала, их количество. Зависимо от количества дополнительных элементов изменяются свойства соединений. К ним относится бор, ванадий, молибден, марганец, титан, углерод, хром, никель, кремний, вольфрам.
Характеристики смесей зависят от их структуры, состава. От этого изменяется прочность, пластичность, температура плавления, плотность, электропроводность и другие параметры. Например, структура чугуна определяет его хрупкость при ударах, больших физических нагрузках.
Свойства и маркировка сплавов
Относительно маркировки, первые цифры, которые идут на маркировке, говорят о процентном содержании углерода в составе. Далее идут заглавные буквы основных легирующих элементов. Начало маркировки могут начинать дополнительные буквы. Они указывают на назначение сплава.
Пластичность и вязкость будут уменьшаться при повышении количества углерода в составе сплава. На другие свойства металлов влияют основные легирующие элементы.
Сферы применения
Этот материл применяется в разных отраслях промышленности:
- Смеси и однородный металл применяются в машиностроении. Из них изготавливаются внутренние детали, корпуса, подвижные механизмы.
- Судостроение, самолётостроение, ракетостроение.
- Строительство — изготовление крепежей, расходных материалов.
- Приборостроение — изготовление электроники для дома.
- Радиоэлектроника — создание элементов для электроприборов.
- Медицина, станкостроение, химическая промышленность.
- Изготовление оружия.
Если для чего-то не подходит однородный материал, подойдут соединения на его основе, характеристики которых значительно отличаются.
Вещества со степенью окисления железа (III)
Свойства соединений железа, в которых оно проявляет степень окисления +3, несколько отличны от рассмотренных выше. Так, характер соответствующего оксида и гидроксида уже не основный, а выраженный амфотерный. Дадим описание основным веществам.
- Оксид железа (III). Порошок мелкокристаллический, красно-бурого цвета. В воде не растворяется, проявляет свойства слабо кислотные, больше амфотерные. Формула: Fe2O3.
- Гидроксид железа (III). Вещество, выпадающее в осадок при действии щелочами на соответствующие соли железа. Характер его выраженный амфотерный, цвет буро-коричневый. Формула: Fe(OH)3.
-
Соли, в состав которых входит катион Fe3+. Таких выделено множество, за исключением карбоната, так как происходит гидролиз и выделяется углекислый газ. Примеры формул некоторых солей: Fe(NO3)3, Fe2(SO4)3, FeCL3, FeBr3 и прочие.
Среди приведенных примеров с практической точки зрения важное значение имеет такой кристаллогидрат, как FeCL3*6H2O, или шестиводный хлорид железа (III). Его применяют в медицине для остановки кровотечений и восполнения ионов железа в организме при анемии
Девятиводный сульфат железа (III) используется для очистки питьевой воды, так как ведет себя как коагулянт.
История – краткая справка
Теорий происхождения слова «железо» несколько, которые во многом зависят от региона и наречия.
Русское наименование, к которому мы все привыкли имеет праславянские корни «želězo», которое в свою очередь видимо произошло из греческого «χαλκός», что в переводе означает «железо и медь».
Но как бы там не было, неоспоримый факт один – применение железа осуществлялось еще в 4 тысячелетии до н.э., т.к. именно этого периода были найдены древние изделия из этого материала.
Популярными историческими изделиями являются украшения из египетских гробниц (более 3000 до н.э.) и кинжал из древнего города Ур (Шумер), откуда согласно Священным Писанием Бог призвал выйти Авраама.
Первый народ, которые начали плавить Fe – хатты, которые проживали на территории Юго-Восточной сегодняшней Турции примерно в 2000 до н.э. Эти сведения археологи получили из древних текстов царя хеттов Анитты, завоевавшего со своим народом хаттов.
Первые сведения о получении из железа стали появились в записях Аристотеля, из легенды об аргонавтах. Народ «Халибы» тщательно промывали речной песок, отсеивая из него тяжелые фракции гематита и магнетита, которые затем в печи переплавляли до получения серебристого нержавеющего металла.
Железо как обозначается в анализе крови
Кроме того, для проведения анализа не требуется специальное оборудование. Однако НСТ тест субъективен, т.к. для оценки его результатов нужен опытный специалист. В связи с этим возможны ложноотрицательные результаты.
Значительное снижение функциональной активности фагоцитов происходит при хронической гранулематозной болезни. Это наследственное хроническое заболевание характеризуется неспособностью фагоцитов уничтожать бактерии. Хроническая гранулематозная болезнь проявляется длительными рецидивирующими (повторяющимися) бактериальными или грибковыми инфекциями, в том числе и опасными для жизни.
Данный анализ позволяет оценить функциональную активность фагоцитов. Анализ помогает диагностировать хроническую гранулематозную болезнь.
Продукты, содержащие феррум
В продуктах питания встречаются 2 вида железа: гемовое и негемовое. Первый вариант – это феррум, входящий в состав гемоглобина. Его источники – вся пища животного происхождения и морепродукты. Гемовое железо быстрее и легче всасывается организмом. Негемовое железо – элемент, полученный из растительных продуктов. Для формирования гемоглобина используется только частично, и то лишь в сочетании с витамином С.
Для достижения максимальной пользы, диетологи рекомендуют совмещать продукты животного и растительного происхождения. Таким способом легко повысить всасывание феррума (иногда до 400 %).
Многим известно, что мясо, особенно красных сортов, а также субпродукты – лучшие источники железа.
Растительная пища также способна дать достаточное количество железа
Правда, для этого важно питаться самыми разными видами еды неживотного происхождения
Исследования частично разрушают теорию о том, что растения не могут обеспечить человека необходимым количеством железа. Во многих вегетарианских продуктах железо содержится в количестве, превышающем 10 % от суточной нормы, а порция шпината или чечевицы обеспечит треть дневной нормы.
Растительная пища содержит меньше калорий и жиров, поэтому идеально подходит для людей, следящих за фигурой и здоровьем. Но, помимо этого, приверженцы вегетарианства не отрицают, что рекомендованная суточная норма железа, полученного исключительно из растительной пищи, должна быть примерно в полтора раза выше, чем у мясоедов.
Среди растительной пищи наилучшими источниками железа являются бобовые и зеленые листовые овощи. Хорошими питательными свойствами и неплохими запасами феррума обладают и цельные зерна. И наиболее неожиданный для многих источник железа – патока из сахарного тростника. Только 1 чайная ложка этого продукта содержит в себе почти 1 миллиграмм железа. Этот показатель значительно превышает таковой среди других подсластителей, таких как мед, кленовый сироп, коричневый сахар.
Чтобы легче понять, какие продукты являются наиболее насыщенными железом, предлагаем таблицу. Используя эти знания, легко избежать железодефицитной анемии.
| Название продукта | Количество | Содержание железа (мг) |
|---|---|---|
| Свиная печень | 200 г | 61,4 |
| Печень говяжья | 200 г | 14 |
| Говяжьи почки | 200 г | 14 |
| Мидии | 200 г | 13,6 |
| Устрицы | 200 г | 12 |
| Сердце | 200 г | 12,6 |
| Мясо кролика | 200 г | 9 |
| Индейка | 200 г | 8 |
| Баранина | 200 г | 6,2 |
| Курица | 200 г | 5 |
| Скумбрия | 200 г | 5 |
| Говяжий фарш (нежирный) | 200 г | 4 |
| Сельдь | 200 г | 2 |
| Яйцо куриное | 1 штука | 1 |
| Перепелиные яйца | 1 штука | 0,32 |
| Черная икра | 10 г | 0,25 |
| Название продукта | Количество | Содержание железа (мг) |
|---|---|---|
| Арахис | 200 г | 120 |
| Соя | 200 г | 10,4 |
| Фасоль (лимская) | 200 г | 8,89 |
| Картофель | 200 г | 8,3 |
| Фасоль белая | 200 г | 6,93 |
| Бобы | 200 г | 6,61 |
| Чечевица | 200 г | 6,59 |
| Шпинат | 200 г | 6,43 |
| Свекла (ботва) | 200 г | 5,4 |
| Кунжут | 0,25 стакана | 5,24 |
| Нут | 200 г | 4,74 |
| Салат ромэн | 200 г | 4,2 |
| Мангольд | 200 г | 3,96 |
| Спаржа | 200 г | 3,4 |
| Брюссельская капуста | 200 г | 3,2 |
| Семена тыквы | 0,25 стакана | 2,84 |
| Тмин | 2 ч.л. | 2,79 |
| Свекла | 200 г | 2,68 |
| Репа | 200 г | 2,3 |
| Порей | 200 г | 2,28 |
| Капуста белокочанная | 200 г | 2,2 |
| Зеленый горошек | 200 г | 2,12 |
| Брокколи | 200 г | 2,1 |
| Оливки | 200 г | 2,1 |
| Кабачок | 200 г | 1,3 |
| Помидоры | 200 г | 0,9 |
| Петрушка | 10 г | 0,5 |
| Перец чили | 10 мг | 1,14 |
| Орегано | 2 ч.л. | 0,74 |
| Базилик | 10 г | 0,31 |
| Черный перец | 2 ч.л. | 0,56 |
По каким признакам можно заподозрить нехватку железа в организме
Признаки анемии – слабость, плохое самочувствие, пониженная работоспособность, головокружение, бледность кожных покровов.
Изменение кожи, волос и ногтей – при нехватке этого вещества кожа шелушится и трескается. Ногти становятся тонкими, а на их поверхности образуются вогнутости и белые поперечные полосы. Волосы теряют блеск и выпадают.
Изменения слизистых. При железодефиците возникает воспаление десен, нёба, языка, в углах рта образуются заеды. Появляется сухость во рту, носу, нарушение глотания.
Необычные вкусовые пристрастия. Больные едят несъедобные предметы – мел, глину, сырое мясо и крупу. Наблюдается пристрастие к резким запахам бензина, растворителя, краски.
Голубоватый оттенок склер – белочной оболочки глаза. При нехватке элемента происходит атрофия глазных тканей, через которые просвечивают сосуды.
Слабость мышц. Больным становится сложно выполнять привычные действия, у них наблюдаются мышечные боли.
Снижение иммунитета. При железодефиците «липнут» инфекции, которые протекают тяжелее обычного.
Тотема
Форма выпуска: раствор для приема внутрь. 1 ампула — 50 мг чистого железа.
Чем лучше жидкая форма?
Тем, что раствор более равномерно распределяется по слизистой пищеварительного тракта, и вероятность ее раздражения уменьшается.
Во-вторых, эта форма хороша для тех, кто не умеет глотать таблетки, или для лежачих больных.
Еще одно преимущество препарата Тотема: в составе более безопасная соль железа — глюконат. Риск побочных меньше.
В-четвертых, Тотема содержит медь и марганец, которые улучшают всасывание железа.
Детям – с 3 мес.
Беременным можно.
Осторожно больным сахарным диабетом, т.к. для вкуса в него добавлено много всякой химической дряни
За это я не люблю жидкие формы. В них, помимо действующих и вспомогательных веществ, необходимых для стабильности, вагон всяких ароматизаторов, красителей, подсластителей и пр., поэтому вероятность аллергических реакций выше.
Как принимать: содержимое ампулы нужно растворить в простой или подслащенной воде и выпить до еды. Для лечения ЖДА принимают по 1-2 ампулы 2 раза в день. Это 100-200 мг железа в сутки.
Признаки нехватки железа в организме
Пониженный процент будет сопутствоваться слабостью, постоянной усталостью, работоспособность снизится; бледностью, сухостью, шершавостью кожного покрова; волосы станут обильно осыпаться; ногти становятся ломкими; пятки и уголки губ покроются неприятные трещины.
Малокровие действует на внешность, и внутреннее состояние тела. Так частым симптом является бледность тканей желудочно-кишечного тракта. Это означает снижение поступления крови, что замедляет работоспособность.
При дефиците системы будут сигнализировать такими проблемами:
- Частое головокружение.
- Человек постоянно чувствует себя уставшим, работать не хочется.
- Конечности немеют.
- Аппетит снижен.
- Глотание затруднено.
- Возникают сбои деятельности ЖКТ.
- Возникает бессонница.
- Ногти ломаются, расслаиваются, часто на поверхности возникают ложкообразные вдавления.
- Даже при легком труде сердце начинает биться ускоренно, появляется отдышка.
- Вкусовые изменение, проблемы с обонянием. Часто люди хотят кушать неприготовленную крупу, нюхать ацетон.
Чтобы точно узнать диагноз лучше в любой лаборатории сдать анализ (общий по крови). Уровень понижения этого микроэлемента для женщины 120 г/л, а у мужчины – 130 г/л.
Почему происходит потеря железа
Существует несколько вариантов нехватки, основные из которых:
- Диета (строгая).
- Потеря крови (обильные месячные).
- Голодание.
- Вегетарианство.
В результате возникнет малокровие, которое обусловлено понижением гемоглобина в жидкости (иногда идет в сочетании с уменьшением эритроцитов в общем массе).
Анемия разделяется на три уровня – средняя, тяжелая и легкая. По статистическим данным более 800 миллионов людей страдают от этой болезни. Зачастую она овладевает молодыми девушками, подростками.
Диагностика дома не возможна, поэтому чтобы выяснить наверняка стоит обратиться к специальным исследованиям в лаборатории. Обращаться к врачу стоит по предварительным симптомам, которые могут возникнуть в период течения заболевания.
Ситуация не будет считаться критической при понижении менее чем на сто г/л. Однако в этот период лучше начать восполнять микроэлемент. Делать это лучше включив в рацион железосодержащие продукты.
Если уровень падает до девяноста г/л, то наступает средняя или тяжелая стадия малокровия. В такой ситуации следует обращаться в больницу за рекомендациями лечащего доктора. При установлении диагноза человеку придется сесть на специальную диету, и принимать лекарства, которые повысят содержание «Iron» в теле.
Ферретаб комп.
Форма выпуска – капсулы пролонгированного действия.
Интересен тем, что в каждой капсуле – три минитаблетки железа (всего 50 мг чистого железа) и одна минитаблетка фолиевой кислоты в хорошей дозировке (500 мкг).
Смотрите:
Полагаю, что сокращение «комп.» в названии препарата означает «комплекс».
Его оптимально рекомендовать при анемии, вызванной дефицитом железа и фолиевой кислоты, и при железодефицитной анемии беременных или для профилактики таковой.
Железо представлено более безопасной, чем сульфат железа, солью – фумаратом. Дает меньше побочных.
Как принимать: натощак по 1 капсуле (50 мг железа) в день. При необходимости врач может увеличить дозировку до 2-3 капсул в день.
Выводы:
Сравнив препараты двухвалентного железа, я пришла к таким выводам:
Наиболее безопасные препараты – Тотема, Ферретаб комп., т.к. они содержат не сульфат железа, а другие соли.
Наиболее адекватные дозировки железа для лечения ЖДА, на мой взгляд, в препаратах Сорбифер Дурулес и Тотема.
Области применения
Железо необходимо при производстве стали, которая имеет широкий диапазон применения. Практически в каждом производстве используется данный материал. Широко применяется железо в быту, его можно встретить в виде кованных изделий и чугуна. Железо позволяет придавать изделию различную форму, поэтому его используют при ковке и создании беседок, ограждений и других изделий.
Пользуются железом все хозяйки на кухне, ведь изделия из чугуна, это не что иное как сплав железа и углерода. Посуда из чугуна равномерно нагревается, долго сохраняет температуру и служит не один десяток лет. В состав практически всех столовых приборов входит железо, а из нержавеющей стали изготовляют посуду и различные кухонные принадлежности и такие необходимые предметы, как лопаты, вилы, топоры и другие полезные приспособления. Широко используется данный металл и в ювелирном деле.
Значение железной руды и сферы, в которых она используется
По преимуществу все отрасли, в которых задействованы эти полезные ископаемые, связаны с металлургической сферой. По большей части руду железа используют при выплавке чугуна с использованием конверторной или мартеновской печи. В свою очередь чугун широко применим во многих промышленных отраслях.
Сегодня крайне популярен и активно изготавливается и другой сверхпрочный, антикоррозийный сплав – сталь, для чего также используются железорудные ископаемые. Это наиболее популярный промышленный сплав, который славится устойчивостью к коррозии и высокой прочностью.
Стальные и чугунные материалы применяют в следующих отраслях:
- ракетостроительная и военная промышленность, производство специальной техники;
- машиностроение, включая изготовление станков и прочих заводских механизмов;
- автомобильное производство (изготавливаются автомобильные рамы, элементы двигателей, корпуса и прочие механические узлы);
- добывающая промышленность (производство тяжёлого добывающего оборудования и прочей спецтехники);
- строительство – армирующие материалы, создание несущего каркаса.
Классификация металлов по температуре плавления
Разные металлы могут переходить в жидкое состояние при разной температуре. Вследствие этого выделяют определённую классификацию. Их делят следующим образом:
- Легкоплавкие — те элементы, которые могут становиться жидкими уже при температуре ниже 600 градусов. К ним относят цинк, олово, свинец и пр. Их можно расплавить даже в домашних условиях — просто нужно разогреть при помощи плиты или паяльника. Такие виды нашли применение в технике и электронике. Они используются для соединения элементов из металла и движения электрического тока. Олово плавится при 232 градусах, а цинк — при 419 градусах.
- Среднеплавкие — элементы, которые начинают расплавляться при температуре от шестисот до тысячи шестисот градусов. Эти элементы используют по большей части для строительных элементов и металлоконструкций, то есть при создании арматур, плит и строительных блоков. В эту группу входят: железо, медь, алюминий. Температура плавления алюминия сравнительно низка и составляет 660 градусов. А вот железо начинает переходить в жидкое состояние лишь при температуре 1539 градусов. Это один из самых распространенных металлов, используемых в промышленности, особенно в автомобильной. Однако железо подвержено коррозии, то есть ржавчине, поэтому ему требуется специальная поверхностная обработка. Его необходимо покрывать краской или олифой, и не допускать попадание влаги.
- Тугоплавкие — это такие материалы, которые расплавляются и становятся жидкими при температуре выше 1600 градусов. В эту группу относят вольфрам, титан, платину, хром и т. п. Они используются в ядерной промышленности и для некоторых машинных деталей. Они могут применяться для расплавки других металлов, изготовления высоковольтных проводов или проволоки. Платину можно расплавить при 1769 градусах, а вольфрам — при 3420 °C.
Единственный элемент, который при обычных условиях находится в жидком состоянии — это ртуть. Температура его плавления составляет минус 39 градусов и его пары являются ядовитыми, поэтому его используют только в лабораториях и закрытых ёмкостях.
Химический состав
Свойства железной руды, ее ценность и характеристики напрямую зависят от ее химического состава. Железная руда может содержать различное количество железа и других примесей. В зависимости от этого выделяют ее несколько типов:
- очень богатые, когда содержание железа в рудах превышает 65%;
- богатые, процент железа в которой варьируется в диапазоне от 60% до 65%;
- средние, от 45% и выше;
- бедные, в которых процент полезных элементов не превышает 45%.
Чем больше побочных примесей в составе железной руды, тем больше необходимо энергии на ее переработку, и тем менее эффективным является производство готовой продукции.
Состав породы может представлять собой совокупность различных минералов, пустой породы и других побочных примесей, соотношение которых зависит от ее месторождения.
Пустая порода также может содержать железо, но ее переработка экономически не целесообразна. Наиболее часто встречающиеся минералы представляют собой оксиды, карбонаты и силикаты железа.
Следует отметить, что в составе железистых пород может содержаться огромное количество вредных веществ, среди которых можно выделить серу, мышьяк, фосфор и другие.
https://youtube.com/watch?v=f09VHpe9R8o